Professionals
voor vrouwen
Klinische toepassing fertiliteitspreservatie bij vrouwen
Een exacte voorspelling van de kans op verminderd of niet functioneren van de ovaria na een gonadotoxische behandeling is tot op heden niet nauwkeurig aan te geven.
Verschillende variabelen spelen hierbij een rol zoals de leeftijd van de patiënt en het soort behandeling. Uit meerdere studies blijkt echter dat de wens tot behoud van fertiliteit voor jonge vrouwen in toenemende mate belangrijk is. Infertiliteit ten gevolge van een gonadotoxische behandeling heeft een grote impact op de kwaliteit van leven. Het tijdig bespreken van de kans op infertiliteit en fertiliteitspreservatie opties is dan ook essentieel en wordt door de ASCO en de British Fertility Society (BFS) aanbevolen. Er zijn verschillende opties voor fertiliteitspreservatie bij vrouwelijke patiënten, die bestaan uit bewezen effectieve en experimentele behandelingen ( zie tabel 1).
Afscherming van de ovaria heeft een geringe effectiviteit door beschadiging als gevolg van strooistaling. Hetzelfde geldt voor transpositie, waarbij een ovarium verplaatst wordt buiten het radiatieveld zonder onderbreking van de oorspronkelijke vascularisatie. Hierbij zijn behalve strooistraling tevens ischaemie en cystevorming complicerende factoren. Het verplaatsen van een ovarium middels transplantatie buiten het radiatieveld is vooralsnog beschreven in case-reports. Hoewel klinisch toepasbaar, is deze techniek voorbehouden aan een derdelijnscentrum met expertise op het gebied van transplantatiechirurgie. Ovariumsupressie tijdens chemotherapie met als doel het verlies van de eicelvoorraad te beperken is alleen in een bepaalde groep patiënten effectief gebleken. Hormoontherapie met behulp van orale anticonceptiva heeft tot op heden niet geleid tot behoud van de ovariële reserve. De ovariële reserve bestaande uit met name primordiale follikels, is niet hormoon-afhankelijk.
Het invriezen van embryo’s is een bewezen effectieve en veilige procedure, zoals toegepast bij de IVF techniek. Vanwege de ruime ervaring die met deze techniek is opgedaan is de kans op een doorgaande zwangerschap 18,6 % per ontdooid embryo. Daarmee heeft deze behandeling waar mogelijk de voorkeur. Nadeel is de noodzaak van hormonale stimulatie ter voorbereiding van het invriezen van de embryo’s, waar 2 tot 3 weken tijd voor nodig is. Indien hormonale stimulatie ongewenst is en/of een partner ontbreekt, is de patiënte aangewezen op cryopreservatie van ovariumweefsel. Deze fertiliteitspreservatie behandeling verkeert nog in de experimentele fase waarbij middels een laparoscopische procedure ovariumweefsel wordt verkregen en ingevroren middels een vaststaand protocol. Anticiperend beleid lijkt gerechtvaardigd vanwege hoopvolle ontwikkelingen. Tot op heden zijn meer dan 100 kinderen geboren, deels na spontaan opgetreden zwangerschappen en deels na IVF na terugplaatsing van ontdooid ovariumweefsel. Toepassingen zoals in vitro maturatie of cryopreservatie van een intact ovarium inclusief de vascularisatie zijn in ontwikkeling. Een vroegtijdige verwijzing naar een gespecialiseerd centrum, voortdurend multidisciplinair overleg en ervaring met fertiliteitspreservatie technieken zijn minimale voorwaarden voor een voorspoedig klinisch traject. Naast het mogelijk voorkomen van infertiliteit lijkt er ook een duidelijk positieve uitwerking van het bespreken en uitvoeren van fertiliteitspresevatie te zijn. Goede en volledige informed consent ten aanzien van overwegingen van behandeling, de prognose en de verwachtingen van de patiënt zijn hierbij vereist.
Door toename van de lange termijn overleving van kinderen en vrouwelijk patiënten met kanker wordt aandacht voor behoud van fertiliteit en kwaliteit van leven belangrijker. Bespreking en uitvoering van fertiliteitspreservatie is verantwoord mits dit in een centrum met expertise, bij voorkeur in een onderzoeksetting, plaatsvindt. Het voorkomen van niet te realiseren verwachtingen en bespreken van de mogelijkheden en risico’s zijn hierbij vereisten. Verder onderzoek ter verbetering van fertiliteitspreservatie is noodzakelijk en onderzoek naar de psychosociale aspecten ervan wordt aanbevolen.
| Periode | Standaard behandeling | Experimentele behandeling |
|---|---|---|
| Voor de puberteit | Ovarium afscherming | Hormoon therapie |
| Ovarium transpositie | ||
| Na de puberteit | Ovarium transpositie | Hormoon therapie |
| Cryopreservatie embryo’s | Cryopreservatie ovariumweefsel | |
| Cryopreservatie eicellen |
Opties voor behoud van vruchtbaarheid bij vrouwen
Veel vrouwen bij wie door ziekte of behandeling de vruchtbaarheid verminderd kan worden, vinden het behoud van hun vruchtbaarheid belangrijk en willen informatie hierover. Maar:
- ze vinden het misschien vervelend om vragen over vruchtbaarheid te stellen:
- ze zijn vaak gefocust op de diagnose en de voorgestelde behandeling en niet in staat na te denken over vruchtbaarheid of de mogelijkheid in de toekomst een gezin te stichten.
- ze zijn misschien niet op de hoogte van het risico op verminderde vruchtbaarheid door hun ziekte en/of behandeling zoals chemotherapie, bestraling (radiotherapie) of operatie
- ze zijn misschien niet op de hoogte van de mogelijkheden voor behoud van de vruchtbaarheid en bang voor bijkomende ingrepen en/of handelingen.
Vrouwen kunnen later spijt krijgen als er geen aandacht is besteed aan het risico voor de vruchtbaarheid, voorafgaand aan een behandeling die de vruchtbaarheid kan verminderen. Door patiënten te informeren over een mogelijk risico, en over mogelijkheden om de vruchtbaarheid veilig te stellen, kan in overleg verwijzing van risicopatiënten naar een fertiliteitsarts of een gynaecoloog met het aandachtsgebied voortplantingsgeneeskunde plaatsvinden. Dit kan het welbevinden en de toekomstige kwaliteit van leven verbeteren. Ook vrouwen met een slechte prognose willen misschien over deze mogelijkheid nadenken en komen hiervoor in aanmerking.
Vruchtbaarheidsbehoud: waar in het behandeltraject?
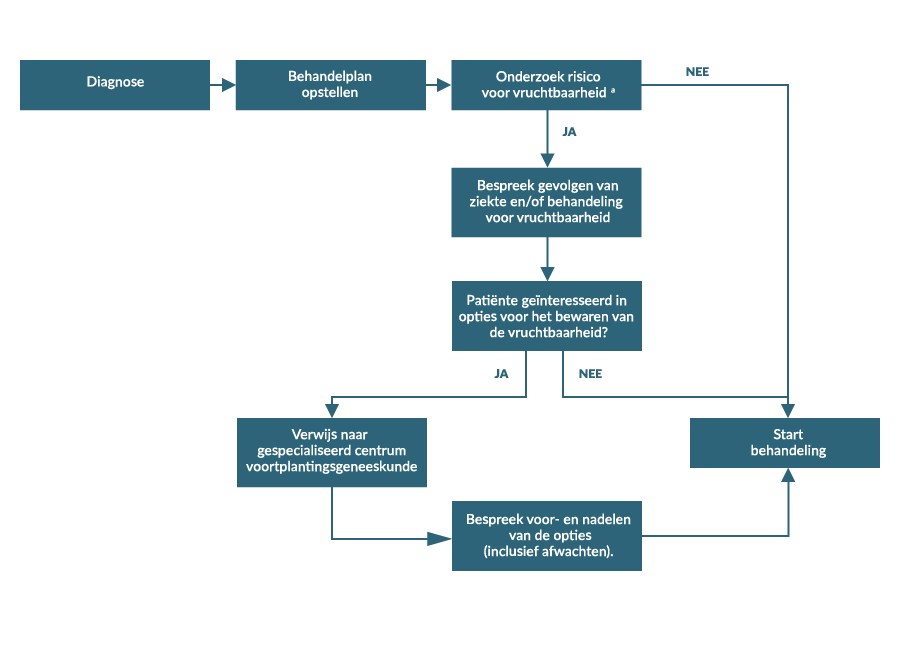
a) Zie onderstaande tabel b) Zie onderstaande afbeelding
Opties voor behoud van vruchtbaarheid
De volgende tabel bevat korte beschrijvingen van de mogelijkheden die beschikbaar zijn voor vrouwen die hun vruchtbaarheid willen behouden.
De SIG Fertiliteitspreservatie-NNF adviseert om patiënten zo vroeg mogelijk door te verwijzen naar een specialist in een gespecialiseerd centrum voortplantingsgeneeskunde, voordat met de behandeling wordt begonnen. Zie de website voor contactgegevens.
Opties voor behoud van vruchtbaarheid bij vrouwen
| Mogelijkheid | Definitie | Tijdstip | Benodigde tijd | Andere overwegingen |
| Opslag van embryo’s | Hormonale stimulatie, eicellen oogsten,bevruchting en embryo’s invriezen voor latere terugplaatsing | Voor de behandeling |
Minimaal 10-14 dagen poliklinische procedure | Semen van partner nodig |
| Opslag van eicellen | Hormonale stimulatie, eicellen oogsten en invriezen voor latere bevruchting en terugplaatsing | Voor de behandeling | Minimaal 10-14 dagen poliklinische procedure | Kan geschikt zijn voor alleenstaande vrouwen |
| Opslag van eierstokweefsel (experimenteel) |
Eierstokweefsel invriezen en terugplaatsen (of in-vitro uitrijping van onrijpe eicellen en bevruchting van eicellen) | Voor de behandeling | Chirurgische ingreep onder algehele anaesthesie in dagopname | Weefsel niet geschikt voor transplantatie bij hoog risico op uitzaaiingen in de eierstok; tot nu toe geen levendgeborenen uit in-vitro uitrijping |
| Stralings- afscherming |
Afscherming van de eierstokken ter vermindering van strooistraling | Tijdens de behandeling | In combinatie met bestraling | Biedt geen bescherming tegen de effecten van chemotherapie |
| Transpositie van de eierstokken |
Chirurgische verplaatsing van de eierstokken buiten het stralingsveld | Voor de behandeling | Chirurgische ingreep of in combinatie met gynaecologische kankeroperatie |
Biedt geen bescherming tegen de effecten van chemotherapie |
| Radicale trachelectomie |
Operatieve verwijdering van de baarmoederhals met behoud van de baarmoeder | Tijdens de behandeling | Chirurgische ingreep met ziekenhuisopname | Beperkt tot baarmoederhalskanker in vroeg stadium |
| Eierstok- onderdrukking (experimenteel) |
GnRH-analogen of-antagonisten voor het onderdrukken van de eierstokken | Tijdens de behandeling | In combinatie met chemotherapie |
Biedt geen bescherming tegen de effecten van bestraling. Geeft (vervelende) bijwerkingen |
Tabel aangepast naar de aanbevelingen van de American Society of Clinical Oncology uit 2006 voor vruchtbaarheidsbehoud bij kankerpatiënten; en Fertile Hope. Cancer and Fertility: Fast Facts for Reproductive Professionals.
Ivf=in-vitrofertilisatie • GnRH=gonadotropin-releasing hormone
Naast de behandelingen die beogen de vruchtbaarheid met gameten van eigen genetisch materiaal te bewerkstelligen, zijn er ook alternatieve methoden van ouderschap.
| Mogelijkheid | Definitie | Tijdstip | Benodigde tijd | Andere overwegingen |
| Donor eicellen | Eicellen gedoneerd door een andere vrouw |
Na de behandeling | Varieert; wordt gedaan in combinatie met hormonale voorbehandeling | Niet-anonieme donatie (bekende of onbekende donor) |
| Donor embryo’s | Embryo’s gedoneerd door een stel | Na de behandeling | Varieert; wordt gedaan in combinatie met hormonale behandeling | Donor embryo’s van IVF kliniek met niet-anoniem donorpaar |
| Adoptie | Proces waarbij een wettelijke ouder-kindrelatie tot stand wordt gebracht |
Na de behandeling |
Varieert afhankelijk van het soort adoptie | Medische voorgeschiedenis kan een rol spelen |
| Pleegzorg | Tijdelijke zorg voor een kind | Na de behandeling | Geen wettelijke ouder-kind relatie. Mogelijk tot leeftijd 42 jaar |
Therapie en het risico op onvruchtbaarheid
De eerste stap naar vruchtbaarheidsbehoud bestaat uit het beoordelen van het risico op onvruchtbaarheid als gevolg van de te starten behandeling (van kanker).
In de volgende tabel zijn diverse behandelschema’s ingedeeld op basis van het bekende risico op onvruchtbaarheid bij vrouwen (gedefinieerd als permanent uitblijven van de menstruatie). Verschillende chemotherapie-schema’s kunnen een ander effect hebben op de vruchtbaarheid. Voor radiotherapie geldt als vuistregel dat 2 Gy de eicelvoorraad al tot de helft kan verminderen bij zowel meisjes als vrouwen (Wallace, 2011) Daarnaast lijkt de leeftijd waarop de bestraling plaatsvindt ook een rol te spelen. Omdat de voorraad onrijpe eicellen bij oudere vrouwen vanwege hun leeftijd al meer is afgenomen, brengt een bepaalde hoeveelheid straling voor een oudere vrouw meer risico’s op onvruchtbaarheid met zich mee dan voor een jongere vrouw. Het definitieve risico op onvruchtbaarheid verschilt dus per patiënt. Raadpleeg hiervoor de betrokken oncologisch behandelaar.
Fertile Hope biedt ook een online risicocalculator die toegankelijk is via hun website (in het Engels).
Voor patiënten die zwanger willen worden, is het belangrijk bij het opstellen van het behandelplan rekening te houden met de leeftijd van de patiënte. Patiënten die ouder zijn dan 35 jaar hebben wellicht minder mogelijkheden voor vruchtbaarheidsbehoud vanwege hun reeds afgenomen eicelvoorraad.
Risico op schade aan de vruchtbaarheid als gevolg van behandelingen
N.B. De weergegeven risico’s in de tabellen zijn slechts een indicatie van het mogelijke risico op vermindering van de vruchtbaarheid als gevolg van een behandeling. Risico’s kunnen per patiënt (leeftijd, exacte dosis medicatie) verschillen. Bovendien gaat het om de initiële behandeling. Het risico verandert indien bij onvoldoende reactie op de initiële behandeling naar een ander schema moet worden overgestapt of wanneer er sprake is van een recidief. Raadpleeg een specialist voor meer specifieke risico’s.
| Type behandeling | Locatie | Risico |
| Operatie | Buiten het onderbuikgebied | Geen |
| Operatie in bekken of onderbuikgebied | Matig | |
| Verwijdering beide eierstokken of baarmoeder Verwijdering 1 eierstok |
Hoog Matig |
|
| Verwijdering hypofyse/hypothalamus* | Hoog | |
| Bestraling | Total Body Irradiation | Hoog |
| Bekken (totale dosis op ovaria) >5 Gy Bekken (totale dosis op ovaria) 2-5 Gy Bekken (totale dosis op ovaria) <2 Gy |
Hoog Matig Laag |
|
| Craniaal (totale dosis) > 24 Gy * | Hoog | |
| Spinaal | Afhankelijk van de dosis die de ovaria bereikt (zie Bekken) | |
| Systemische behandeling | ABVD (Adriamycine, Bleomycine, Vinblastine, Dacarbazine) | Laag |
| Alkylerende chemotherapie bij conditionering voor (beenmerg)transplantatie | Hoog | |
| AC (Adriamycine, cyclofosfamide) >40 jaar >30 jaar |
Matig Laag |
|
| Bevacizumab | Onbekend | |
| Cetuximab | Onbekend | |
| CMF, FEC, FAC kuren (6 cycli) > 40 jaar > 30-39 jaar < 30 jaar |
Hoog Matig Laag |
|
| Cyclofosfamide (totale dosis) >7.5 gram/m2 | Hoog | |
| Cyclofosfamide (totale dosis) >5 gram/m2 >40 jaar <40 jaar |
Hoog Matig |
|
| Erlotinib | Onbekend | |
| Imatinib | Onbekend | |
| Interferon alpha | Geen | |
| Irinotecan | Onbekend | |
| Methotrexaat 5-fu | Geen | |
| NOVP (Novantrone, Oncovin, Vinblastine, Prednison) | Laag | |
| OEPA (Oncovin,etoposide, prednison, adriamycine) | Laag | |
| Oxaliplatine | Onbekend | |
| Procarbazine protocollen (MOPP, MVPP, COPP, ChlVPP, BEACOP) | Hoog | |
| Radioactief jodium | Geen | |
| Tamoxifen | Hoog (voor de duur van het gebruik) | |
| Taxanen (Paclitaxel, Docetaxel) | Onbekend | |
| Trastuzumab | Onbekend | |
| Vincristine | Geen |
* Hormonale suppletie mogelijk. Consulteer een endocrinoloog.
Tabel aangepast naar de aanbevelingen van de American Society of Clinical Oncology uit 2006 voor vruchtbaarheidsbehoud bij kankerpatiënten; Fertile Hope. Cancer and Fertility: Fast Facts for Reproductive Professionals; en Meirow D, et al. Clin Obstet Gynecol. 2010;53:727-739.
Bronnen
Voor meer informatie over risico op onvruchtbaarheid en over mogelijkheden voor vruchtbaarheidsbehoud voor vrouwen met kanker en over doorverwijzen van patiënten naar een specialist op het gebied van vruchtbaarheidsbehoud:
- www.adoptie.nl
- American Society for Reproductive Medicine (in het Engels)
- www.borstkankerenkinderwens.nl
- www.deverdwaaldeooievaar.nl
- Fertile Hope (in het Engels)
- www.fiom.nl
- www.freya.nl
- The Hormone Foundation® (in het Engels)
- www.nnf-info.nl
- Oncofertility Consortium®(in het Engels)
- www.pleegzorg.nl
- https://richtlijnendatabase.nl/richtlijn/fertiliteitsbehoud_bij_vrouwen_met_kanker/inleiding.html
- SaveMyFertility, een gezamenlijke informatiebron van het Oncofertility Consortium® en The Hormone Foundation® (in het Engels)
Referenties
- Ethics Committee of the American Society for Reproductive Medicine. Fertility preservation and reproduction in cancer patients. Fertil Steril. 2005;83:1622-1628.
- Fertile Hope. Cancer and Fertility: Fast Facts for Reproductive Professionals. 2008.
- Jeruss JS, Woodruff TK. Preservation of fertility in patients with cancer. N Engl J Med. 2009;360:902-911.
- Lee SJ, Schover LR, Partridge AH, et al. American Society of Clinical Oncology recommendations on fertility preservation in cancer patients. J Clin Oncol. 2006;24:2917-2931.
- Meirow D, Biederman H, Anderson RA, Wallace WH. Toxicity of chemotherapy and radiation on female reproduction. Clin Obstet Gynecol. 2010;53:727-739.
- Thewes B, Meiser B, Taylor A, et al. Fertility- and menopause-related information needs of younger women with a diagnosis of early breast cancer. J Clin Oncol. 2005;23:5155-5165.
- Tschudin S, Bitzer J. Psychological aspects of fertility preservation in men and women affected by cancer and other life-threatening diseases. Hum Reprod Update. 2009;15:587-597.
- Wallace, WHB. Oncofertility and preservation of reproductive capacity in children and young adults. Cancer. 2011;117:2301-2310.
- Woodruff TK. The Oncofertility Consortium—addressing fertility in young people with cancer. Nat Rev Clin Oncol. 2010;7:466-475.
Online keuzehulp bij kanker
Deze keuzehulp is er voor jonge vrouwen met kanker die voor de beslissing staan om een vruchtbaarheidssparende behandeling te ondergaan. Meer informatie hierover vind je hier.
De website keuzehulp-vruchtbaarheidsbehoud-kanker is in het leven geroepen om patiënten te informeren over de mogelijkheden om de vruchtbaarheid te proberen te sparen voorafgaand aan een behandeling van kanker, en hen voor te bereiden op het nemen van een beslissing daarover samen met hun arts.